Биоэнергетика, фотосинтез и молекулярные машины живой клетки
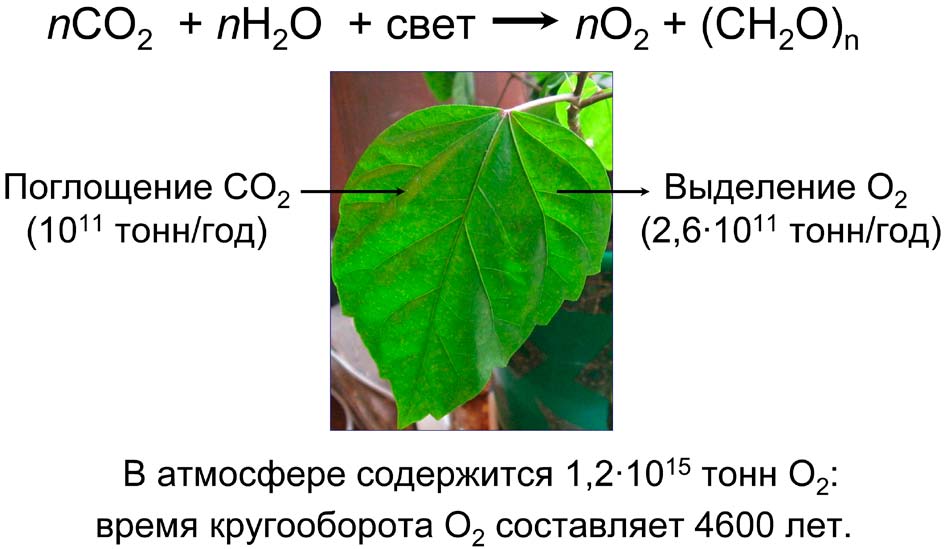
Биоэнергетика — наука о преобразовании и запасании энергии внешних источников (солнечный свет, продукты питания), обеспечивающих все разнообразие жизни в биосфере Земли. Началом биоэнергетики принято считать август 1771 года, когда английский ученый Джозеф Пристли (1733-1804) обнаружил, что растения могут «исправлять» свойства воздуха, меняющего свой состав в результате горения или жизнедеятельности животных. Пристли показал, что в присутствии растений «испорченный» воздух снова становится пригодным для горения и поддержания жизни животных. В ходе дальнейших исследований (Ингенгауз, Сенебье, Соссюр, Буссенго и др.) было установлено, что растения при освещении поглощают из воздуха углекислый газ и выделяют в атмосферу молекулярный кислород (О2). Эти процессы, названные фотосинтезом, обеспечивают биосферу Земли кислородом (рис. 1). Из углекислого газа, поглощаемого из атмосферы, и воды растения синтезируют органические вещества. Роберт Майер, открывший закон сохранения энергии, в 1845 году написал, что растения превращают энергию солнечного света в энергию химических соединений, образующихся при фотосинтезе. По его словам, «распространяющиеся в пространстве солнечные лучи “захватываются” и сохраняются для использования в дальнейшем по мере надобности». Впоследствии К.А. Тимирязевым и другими исследователями было показано, что важнейшую роль в использовании растениями энергии солнечного света играют молекулы хлорофилла, входящего в листья растений. Образующиеся при фотосинтезе углеводы (сахара) используются как источник энергии и строительный материал для синтеза различных органических соединений у растений и животных. Фотосинтез включает в себя большое число фотофизических и биохимических процессов, в результате которых растения синтезируют углеводы (сахара) за счет энергии солнечного света. У растений процессы фотосинтеза протекают в хлоропластах — энергопреобразующих органеллах растительной клетки. Важнейшим продуктом световых стадий фотосинтеза являются молекулы аденозинтрифосфата (АТФ). Молекулы ATФ служат универсальным источником энергии, своеобразной энергетической «валютой» в клетках растений, бактерий и животных.
В настоящее время установлен химический состав и выяснено пространственное строение белковых комплексов, обеспечивающих трансформацию энергии при фотосинтезе. В расшифровке всей совокупности фотофизических и фотохимических процессов фотосинтеза ключевую роль сыграли современные физические методы: (а) рентгеноструктурный анализ, позволивший расшифровать пространственное строение огромных белковых комплексов фотосинтетического аппарата на уровне отдельных атомов; (б) лазерные методы, позволяющие изучать рекордно быстрые фотофизические процессы (поглощение света и миграция энергии между светособирающими пигментами); (в) методы абсорбционной спектроскопии и электронного парамагнитного резонанса, позволяющие регистрировать движение заряженных частиц (электроны и протоны) вдоль своеобразных «электронных проводов», образованных биомолекулами.
|
У всех фотосинтетических организмов структурно-функциональным звеном фотосинтетического аппарата является фотосистема — пигмент-белковый комплекс, который содержит пигменты светособирающей антенны, фотореакционный центр и связанные с ним молекулы — переносчики электронов и протонов. Поглощение света молекулами хлорофилла или вспомогательных |
|
|
Рис. 1. Общее уравнение фотосинтеза |
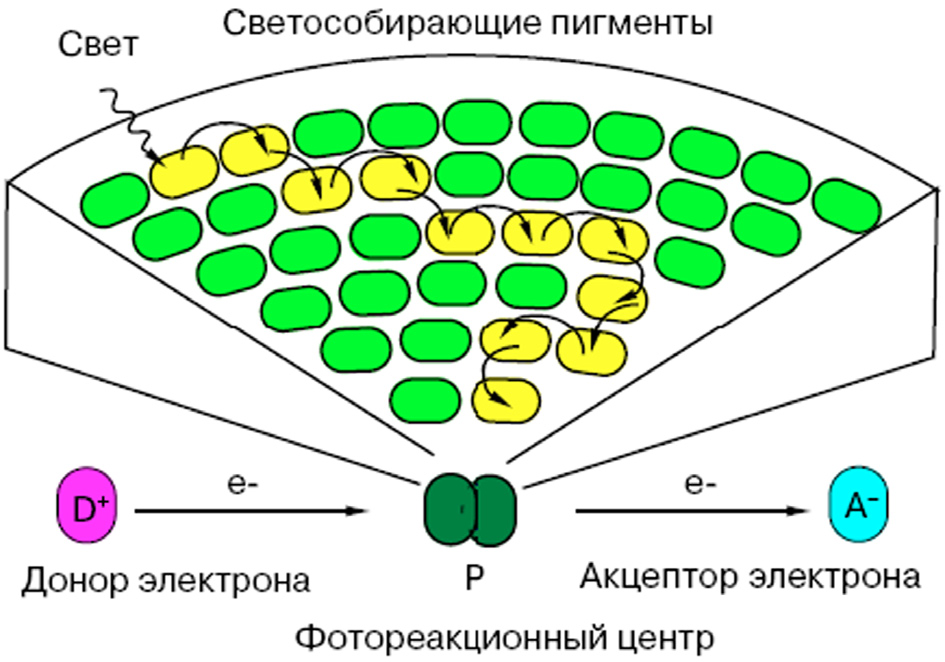
пигментов является первым актом фотосинтеза. Ансамбль пигментов, входящих в светособирающую антенну, эффективно улавливает солнечный свет и направляет его энергию к фотореакционному центру. Энергия кванта света, поглощенного одной молекулой пигмента, мигрирует по пигментной матрице до тех пор, пока в конечном итоге возбуждение не попадет на фотореакционный центр P. Подобно тому, как жидкость стекает со стенок широкой воронки к ее узкому горлышку, к фотореакционному центру Р направляется энергия света, поглощаемого многими молекулами светособирающих пигментов (схематическое изображение этого процесса показано на рис. 2). На один фотореакционный центр приходится большое количество молекул хлорофилла (200-400), что обеспечивает достаточно частое срабатывание реакционного центра даже при относительно слабой интенсивности света, поглощаемого листьями в условиях затенения растения. Это увеличивает сбор света. Тенелюбивые растения имеют, как правило, больший размер светособирающей антенны по сравнению с растениями, произрастающими в условиях высокой освещенности. Аналогичный принцип позаимствовали у природы радиофизики и астрофизики — для улавливания
|
|
слабых сигналов используют антенны более крупных размеров. Эффективность миграции энергии в антенне к реакционному центру исключительно велика потому, что светособирающая антенна представляет собой упорядоченную структуру, обеспечивающую очень хорошее взаимодействие пигментов друг с другом. Благодаря этому потери энергии поглощаемых квантов света в тепло или в излучение очень малы (КПД ? 96-98%). |
|
Рис. 2. Схема миграции энергии в светособирающей антенне |
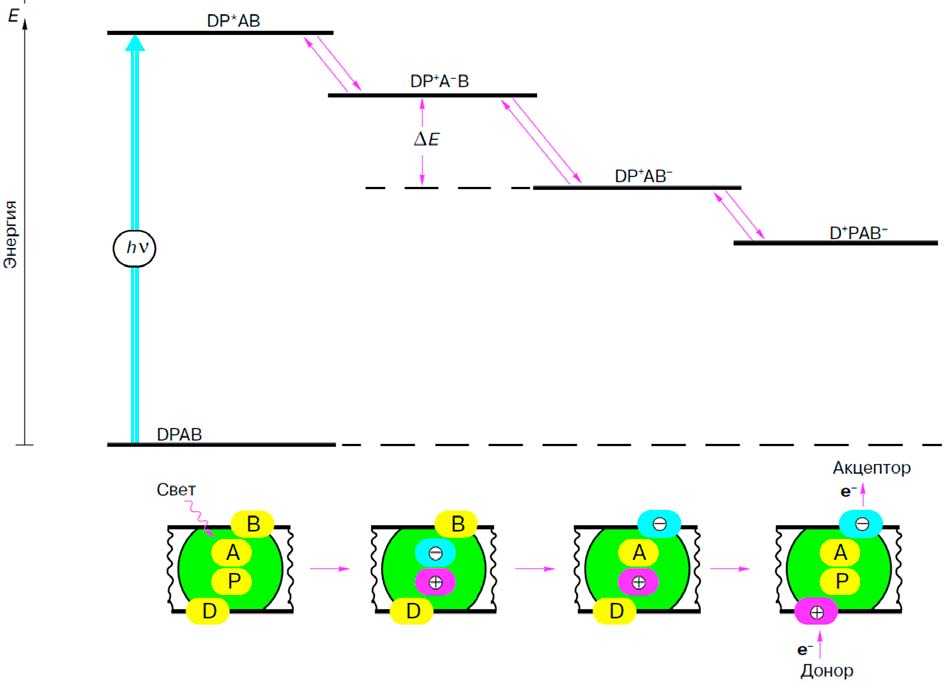
Фотореакционный центр P содержит особую пару молекул хлорофилла, он играет роль ловушки энергии возбуждения, мигрирующего по светособирающей антенне. В результате очень быстрого переноса электрона от возбужденного центра P* к молекуле первичного акцептора электрона A (? 10-13 – 10-12 с) реализуется второй важный этап преобразования солнечной энергии при фотосинтезе — разделение зарядов в реакционном центре. При этом образуются сильный восстановитель A– (донор электрона) и сильный окислитель P+ (акцептор электрона). Заряженные молекулы P+ и A– расположены в мембране асимметрично: в хлоропластах P+ находится ближе к внутренней поверхности мембраны, а акцептор A– расположен ближе к внешней стороне (рис. 3). В результате разделения зарядов (электрон переносится от Р к А) на мембране возникает разность электрических потенциалов ?? = ?in – ?out > 0. Это явление аналогично генерации разности электрических потенциалов в фотоэлементе. Эффективность работы фотореакционных
|
центров очень высока: КПД разделения зарядов составляет, как правило, не менее 90–95%. Стабилизация разделенных зарядов обусловлена за счет других реакций электронного транспорта: от первичного акцептора A– электрон очень быстро (за время ~10-12 – 10-11 с) уходит на другой акцептор электрона B (D(P+A–)B ? D(P+A)B–) и далее электрон перемещается по сравнительно длинной цепи переноса электронов к конечному акцептору. Эту цепь можно уподобить своеобразному белковому проводу. |
|
|
Рис. 3. Схематическая диаграмма изменений энергии в фотореакционных центрах |
При этом электрон не только удаляется от положительно заряженного центра P+, но при этом заметно снижается энергия всей системы (рис. 3). Такая потеря энергии — это своеобразный энергетический «налог», которые обеспечивает сохранение разности потенциалов (уменьшается вероятность рекомбинации зарядов).
В результате работы фотореакционных центров, преобразующих энергию квантов света в энергию разности потенциалов на фотосинтетической мембране, электроны «забираются» от молекул воды (это происходит в так называемых водорасщепляющих комплексах) и переносятся к фотореакционным центрам. При этом выделяется молекулярный кислород, который попадает в атмосферу (мы дышим за счет этого кислорода!). Появление фотосинтезирующих организмов, способных разлагать воду, явилось одним из важнейших этапов развития живой природы на Земле. Фотосинтезирующие организмы, «научившись» в ходе биологической эволюции разлагать воду за счет энергии солнечного света, овладели неисчерпаемым источником электронов для энергообеспечения различных биохимических процессов. Разлагая воду, фотосинтезирующие организмы оксигенного типа (цианобактерии, водоросли, высшие растения) наполнили атмосферу Земли молекулярным кислородом. Таким образом, на Земле возникли благоприятные условия для бурного эволюционного развития организмов, энергетика которых связана с дыханием (потребление кислорода).
Другой важнейший «продукт» световых стадий фотосинтеза — разность потенциалов, которая служит источником энергии для работы АТФ-синтазы — макромолекулярной «машины» (рис. 4), осуществляющей синтез молекул АТФ. Молекулы АТФ — универсальная энергетическая «валюта» живой клетки. Понятие «молекулярные машины», в настоящее время стало общепринятым, оно прочно утвердилось в научной литературе [1–7]. Молекулярная машина — макромолекулярное устройство (молекула белка, белковый комплекс или химические структуры искусственного происхождения), которое осуществляет преобразование химической или электрохимической энергии в энергию направленного молекулярного движения. Среди основоположников научного направления, связанного с разработкой концепции «машинных» механизмов функционирования белков и макромолекулярных комплексов, был Лев Александрович Блюменфельд (1921–2002), выдающийся биофизик, столетие со дня рождения которого будет отмечаться 23 ноября 2021 года. В течение многих лет Л.А. Блюменфельд возглавлял кафедру биофизики физического факультета МГУ. Эта кафедра — первая в мире кафедра биофизики, созданная на физическом факультете университета. На рубеже 60–70-х годов прошлого столетия Л.А. Блюменфельд выдвинул и обосновал «релаксационную» гипотезу ферментативного катализа и преобразования энергии в биологических системах. В основе этой гипотезы лежат представления о том, что важнейшую роль в работе ферментов и макромолекулярных комплексов играют сравнительно медленные структурные перестройки макромолекул, определяемые их механическими степенями свободы.

Профессор Лев Александрович Профессор Лев Александрович
Блюменфельд и академик Блюменфельд
Игорь Евгеньевич Тамм
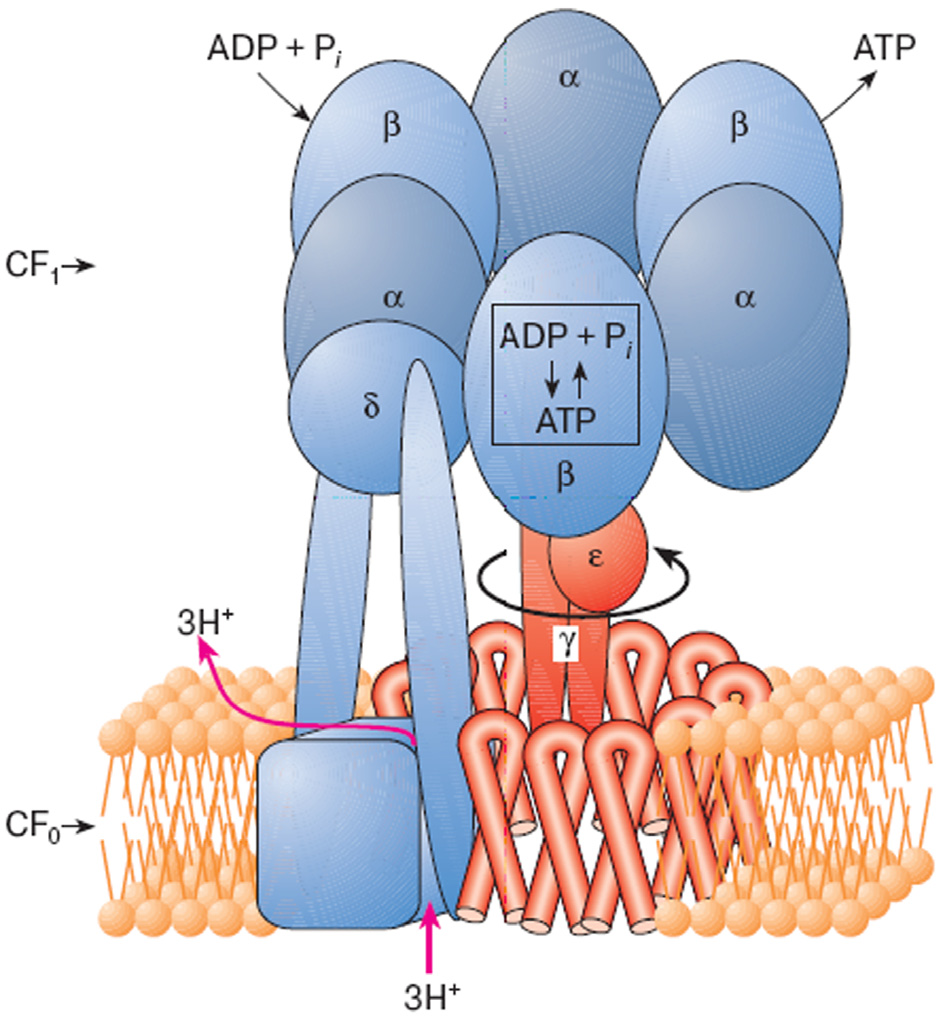
АТФ-синтаза — наиболее яркий пример обратимой молекулярной машины, работающей как электромотор-генератор [6,7]. За счет разности электрических потенциалов, создаваемой на энергопреобразующей мембране, происходит трансмембранный перенос протонов (электрический ток) через АТФ-синтазу (рис. 4), вызывающий направленное вращение ротора и обеспечивающий протекание химической реакции (синтез АТФ). Гидролиз (распад) АТФ вызывает вращение ротора электромотора в обратном направлении, приводящее к генерации разности потенциалов на мембране. Таким образом, получается полная аналогия с работой макроскопического электромотора или генератора, режим работы которого определяется направлением вращения ротора: вращение ротора в одну сторону — механическая работа, вращение ротора в противоположном направлении — генерация разности потенциалов. АТФ-синтазу можно рассматривать как молекулярный электромотор-генератор, состоящий из статора и ротора. Статор включает в себя гексамер ?3?3 и связанную с ним субъединицу ?, а также мембранную субъединицу a и две субъединицы b, выполняющие роль своеобразных «кронштейнов», удерживающих статор относительно мембраны (рис. 4). Получены многочисленные и очень убедительные экспериментальные доказательства того, что каталитическая активность АТФ-синтазы связана с вращением ее «ротора», состоящего из кольца cn и белковых субъединиц ? и ?. Считается, что вращение субъединицы ? внутри комплекса ?3?3, происходящие за счет энергии разности электрохимических потенциалов протонов, вызывает согласованное изменение конформации трех каталитических субъединиц ?, что в конечном итоге обеспечивает работу фермента — синтез АТФ (см. подробнее обзорные статьи [1-7]). Исследования кинематических характеристик этого мотора показали, что чем выше механическая нагрузка на мотор, тем реже происходят скачкообразные повороты «ротора» (мотор крутится медленнее). Например, средняя скорость вращения белкового «хвоста», пришитого к ротору, уменьшается с увеличением его длины, так как при этом возрастает гидродинамическое сопротивление. Отличительной особенностью вращающегося электромотора АТФ-синтазы является его исключительно высокий коэффициент полезного действия.
|
Количественные оценки работы мотора против силы вязкого трения позволили определить коэффициент его полезного действия. Оказалось, что работа, которую совершает мотор при повороте ротора на 120°, почти в точности равна энергии, выделяющейся при гидролизе одной молекулы АТР (КПД мотора близок к 100%). Таким образом, идея о том, что молекула белка работает как макромолекулярная машина, в настоящее время уже не воспринимается как экзотический вымысел биофизиков, выдвинувших эту гипотезу более 45 лет назад, она нашла убедительное доказательство и вошла в золотой фонд современной биофизики. |
|
|
Рис. 4. Схематическое строение АТФ-синтазы |
1. Блюменфельд Л.А. // Проблемы биологической физики. М.: Наука. 1974.
2. Твердислов В.А., Тихонов А.Н., Яковенко Л.В. Физические механизмы функционирования биологических мембран. Изд-во МГУ, 1987.
3. Кукушкин А.К., Тихонов А.Н. Лекции по биофизике фотосинтеза высших растений. Изд-во МГУ, 1988.
4. Blumenfeld L.A., Tikhonov A.N. // Biophysical Thermodynamics of Intracellular Processes. Molecular Machines of the Living Cell. N.Y: Spinger. 1994.
5. Чернавский Д.С., Чернавская Н.М. // Белок-машина: Биологические и макромолекулярныt конструкции. М.: Янус-К, 1999.
6. Романовский Ю.М., Тихонов А.Н. // Молекулярные преобразователи энергии живой клетки. Протонная АТР-синтаза — вращающийся молекулярный мотор. — Успехи физических наук, Том 180, № 9, стр. 931-956 (2010).
7. Tikhonov A.N. pH-Dependent regulation of electron transport and ATP synthesis in chloroplasts // Photosynthesis Research, 116, 511-534 (2013).
Профессор А.Н. Тихонов